O teste padrão para o diagnóstico da COVID-19 é o RT-qPCR. O primeiro passo para entender esse termo é traduzi-lo corretamente. RT significa “reverse transcription” e qPCR significa “quantitative PCR”, que é sinônimo de “real-time PCR”.
Para a realização do RT-qPCR, são seguidas as seguintes etapas:
- Extração de RNA
- Retrotranscrição de RNA em cDNA (RT-PCR)
- Amplificação do cDNA em equipamento que capta o sinal a cada ciclo, por 40 ciclos (qPCR)
O que esperamos observar após o término de um experimento de PCR simples?

Bandas num gel de agarose. Cada coluna representa uma amostra.
O que esperamos observar após o término de um experimento de qPCR?
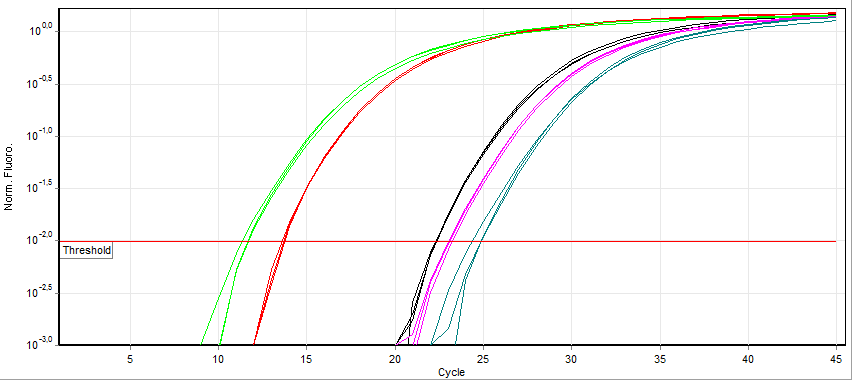
Uma planilha de Excel com valores numéricos, indicando o número de ciclos necessários para o início da detecção em cada amostra, o que recebe o nome de Ct ou Cq. Esses números são derivados de curvas de detecção, representadas num gráfico onde cada linha representa uma amostra.
Enquanto os dados de PCR simples permitem dizer se uma amostra está presente ou não, os dados de um PCR quantitativo permitem dizer não apenas se a amostra está presente, mas a quantidade inicial dessa amostra, baseado no número de ciclos necessários para o início da detecção (quanto mais ciclos são necessários, menor a quantidade inicial da amostra).
Contudo, dado que tanto o PCR simples como o PCR quantitativo podem dizer se a amostra está presente, por que o qPCR é a primeira escolha para o diagnóstico? Porque o tempo de realização de um experimento de qPCR é menor e a sua sensibilidade é maior. O custo é maior? Sim, mas torna-se menos relevante quando se trabalha em larga escala.
PCR convencional
- Capacidade máxima de amostras por experimento: 40 amostras
- Um gel de agarose: $R\$$2,30, ou $R\$$0,05 por amostra (1 kg = $R\$$460, dá para fazer 200 experimentos com 5 g em cada)
- Extração de RNA: $R\$$35 por amostra (kit de extração de 50 amostras de RNA: 350 dólares = $R\$$1750)
- Transcrição reversa: $R\$$25 por amostra (kit de transcriptase reversa para 50 amostras: $R\$$1250)
- Um par de primers para COVID: $R\$$0,14 por amostra ($R\$$170 um par de primers que realizam no mínimo 1200 reações)
- dNTP para PCR simples: $R\$$0,60 por amostra (1 mL custa 123 dólares e faz mil reações)
Total: $R\$$60,79 por amostra
Volume de amostras por experimento: 40 amostras ($R\$$2.400 por experimento)
Custo de equipamentos: $R\$$33,5 mil ($R\$$20.000 termociclador, $R\$$500 bacia de eletroforese, $R\$$9.000 ultravioleta, $R\$$4.000 kit de pipetas), equivalente a $R\$$280 por mês, por 10 anos.
PCR quantitativo
Não usamos o gel de agarose, nem a amplificação prévia (-$R\$$0,65), mas usamos:
- Um mix de SYBR Green: $R\$$4,42 por amostra (1 mL custa 88,5 dólares e faz 100 reações)
- Uma placa descartável de 96 amostras: $R\$$0,38 por amostra (20 placas custam 145 dólares)
Total: $R\$$64,94 por amostra
Volume de amostras por experimento: 96 amostras ($R\$$6.234 por experimento)
Custo de equipamentos: $R\$$194 mil ($R\$$20.000 termociclador, $R\$$170.000 PCR Tempo-Real, $R\$$4.000 kit de pipetas), equivalente a $R\$$1600 por mês, por 10 anos.
O custo unitário de um PCR quantitativo é apenas um pouco maior que o custo unitário do PCR convencional (+6,8%), mas o custo unitário de alguns insumos assustam (custo do SYBR Green e da placa descartável), além do alto custo dos equipamentos, para quem pretende montar um laboratório. Um equipamento de Real-Time PCR não apenas é mais caro, como requer manutenção especializada, o que adiciona um custo adicional.
Contudo, tirando a questão do custo, há estudos que mostram que o qPCR pode detectar quase duas vezes mais que um PCR convencional, além de ser um procedimento mais rápido. Dentre os convencionais, o semi-nested PCR se mostrou o mais sensível.
Limitações
A sensibilidade do RT-qPCR depende do período da doença em que o material é coletado.
- 1/22 testam negativo após 1 semana de sintomas (4,5%)
- 11/43 testam negativo após 2 semanas (25,6%)
- 38/68 testam negativo após 3 semanas (55,9%)
- 68/91 testam negativo após 4 semanas (74,7%)
- 51/58 testam negativo após 5 semanas (87,9%)
O tempo médio de liberação viral é de cerca de 15,7±6,7 dias em pacientes não internados na UTI e 22,2±3,6 dias em pacientes internados na UTI. Outro estudo encontrou um tempo médio de liberação viral de 17 dias após o início dos sintomas, mas em alguns casos pode demorar mais de 30 dias. Em cerca de 21% dos casos, pode haver nova positivação do teste mesmo após dois testes consecutivos negativos.
Outros métodos de amplificação de DNA
Há o PCR digital (dPCR), que tem ótimo desempenho para amostras com pouco material nucleico. O custo estimado por amostra de dPCR é ~$R\$$30.
Há um outro procedimento de amplificação de DNA altamente sensível chamado LAMP, feito numa reação isotérmica, com resultados visíveis a olho nu e à beira do leito, em 5-10 minutos.